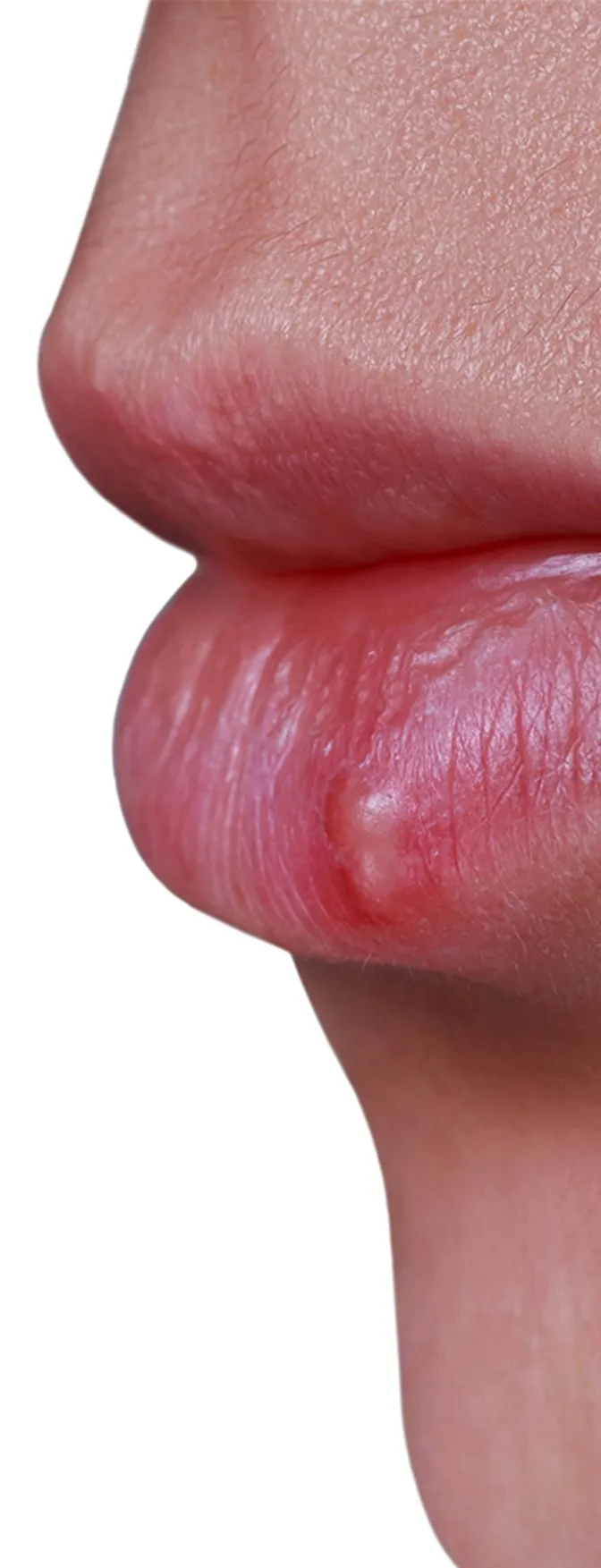
Neuen Erkenntnissen zufolge, bewegt sich das Virus wie auf Schienen zum Zellkern.
Lediglich mit einem Kuss wird Herpes Typ 1 für ein ganzes Leben besiegelt. Einmal angesteckt, wird man es nicht mehr los. Mehr als die Hälfte der Erwachsenen sind Träger von HSV (Herpes Simplex Virus), das im peripheren Nervensystem überwintert und nie ausgerottet werden kann. Eine neue Studie hat die heimtückische Strategie des Virus für die Infektion des Nervensystems aufgedeckt. Damit könnte ein Weg hin zur Entwicklung eines Impfstoffes sowohl gegen HSV1 als auch seinen Geschwistertyp HSV2 geschaffen sein.
Die meisten Träger werden von HSV1 nicht mehr abbekommen als eine lästige Fieberblase. Bei anderen jedoch kann das Virus bis hin zur lebensbedrohlichen Enzephalitis führen. Es gibt auch immer mehr Hinweise, dass es zu Demenz beiträgt.
HSV2 wiederum wird eher durch sexuellen Kontakt übertragen. Während des Geburtsvorgangs kann es als Neugeborenenherpes von der Mutter auf das Baby übertragen werden. In den schlimmsten Fällen kann die Krankheit das Gehirn schädigen oder sich in allen Organen ausreiten und tödlich sein.
Impfstoff benötigt
"Wir benötigen dringend einen Impfstoff, der verhindert, dass Herpes in das Nervensystem eindringt", betont der Mikrobiologe und Immunologe Greg Smith von der Northwestern University Feinberg School of Medicine in Chicago in der im Fachblatt "Nature" publizierten Arbeit.
Die Forscher entdeckten, wie Herpes ein Protein aus Epithelzellen entführt und es in einen Überläufer, damit es in das periphere Nervensystem gelangen kann. Diese Entdeckung könnte weitreichende Folgen für viele Viren haben, darunter auch HIV und sogar Sars-CoV-2, so Smith. "Das Virus muss seinen genetischen Code in den Zellkern injizieren, damit es weitere Herpesviren produzieren kann", erklärt der Forscher. "Es programmiert die Zelle so um, dass sie zu einer Virenfabrik wird. Die große Frage ist, wie es in den Kern eines Neurons gelangt."
Wie viele Viren lässt sich auch Herpes transportieren. Wie auf Schienen bewegt es sich bis zum Kern eines Neurons. Dabei nutzt es Proteinmotoren, die Dynein und Kinesin genannt werden.
"Indem wir gelernt haben, wie das Virus diese unglaubliche Leistung vollbringt, um in unser Nervensystem einzudringen, können wir nun darüber nachdenken, wie wir ihm diese Fähigkeit nehmen können", beschreibt Smith. "Wenn man es daran hindern kann, Kinesin zu assimilieren, hätte man ein Virus, das das Nervensystem nicht mehr infizieren könnte. Und dann hätte man einen Kandidaten für einen präventiven Impfstoff."
Die Reise durchs Land
Man kann sich die Zelle wie einen Bahnhof vorstellen, skizzieren die Wissenschafter in der Publikation. Alle Gleise führen zu einem Knotenpunkt, dem sogenannten Zentrosom. Es gibt zwei Arten von Zugmaschinen, die Proteine Dynein und Kinesin. Die eine fährt in Richtung des Knotenpunkts - zum Beispiel in die Innenstadt - und die andere führt von dort weg in die Vororte.
Infiziert ein typisches Virus die Schleimhautzellen in Nase und Mund, schnappt es sich beide Lokomotiven und bewegt sich auf sogenannten Mikrotubuli-Bahnen hin und her, bis es schließlich mehr oder weniger zufällig im Zellkern ankommt. Alles in allem ist der Weg von der Vorstadt zum Zellkern über das Zentrosom ein kurzer Weg.
Die Reise durch die Nerven ist allerdings das Äquivalent einer Reise quer durchs Land. Herpes springt für diese Tour auf den Dynein-Motor, sorgt aber auch dafür, dass die Kinesin-Motoren ihn nicht mit auf den Weg zurücknehmen, den er gekommen ist.
"Es ist ein langer Weg", erklärt Smith. "Es dauert wahrscheinlich acht Stunden, um vom Ende des Neurons zum Zentrum zu gelangen. Doch der Dynein-Motor kann es nicht weiter als bis zur Nabe bringen. Und Herpes muss den Zellkern erreichen. Dazu greift das Virus in seine "Tasche" und holt einen Kinesin-Motor heraus, den es aus den Schleimhautzellen entführt und davon überzeugt hat, Teil seines Teams zu werden. In einem Akt des Verrats transportiert dieses assimilierte Kinesin es direkt zum Zellkern, skizziert der Mikrobiologe äußerst bildlich.
"Dies ist die erste Entdeckung eines Virus, das ein zelluläres Protein umfunktioniert und des für nachfolgende Infektionsrunden nutzt", so Erstautorin Caitlin Pett aus dem Smith-Labor.